Benzene là một hợp chất hữu cơ có công thức hoá học C6H6. Benzen là một hyđrocacbon thơm, trong điều kiện bình thường chính là một chất lỏng chưa màu, mùi dịu ngọt dễ chịu, dễ cháy. Benzen tan kém trong nước , rượu Vì chỉ chứa carbon và hydro nên benzene là một hydrocarbon.
Benzen chính là thành phần thiên nhiên của dầu thô , là một trong những hóa chất dầu cơ bản. Do các liên kết pi thường xuyên tuần hoàn giữa các nguyên tử carbon, benzen đã được phân loại là hydrocarbon thơm, [n] – annulene ( – annulene) thứ hai. Nó đôi khi đã được viết tắt chính là PhH. Benzen chính là một chất lỏng không màu , và rất dễ cháy , có mùi thơm, nó gây ra mùi thơm xung quanh các trạm xăng. Nó được sử dụng chủ yếu như một tiền chất để sản xuất các hóa chất có cấu trúc phức tạp hơn, chẳng hạn như ethylbenzene và cumene, trong đó hàng tỷ kg được sản xuất hàng năm. Vì benzen có số octan cao, các dẫn xuất thơm như toluene , và xylene thường chiếm tới 25% xăng. Bản thân benzen đã bị giới hạn ở mức dưới 1% trong xăng vì nó chính là chất gây ung thư ở người. Hầu hết các ứng dụng phi công nghiệp cũng bị tránh vì nguyên do tương tự.
Từ “benzen” có nguồn gốc từ “nhựa benzoin”, một loại nhựa thơm được các dược sĩ , và nước hoa châu u biết đến từ thế kỷ 16 như một sản phẩm của Đông Nam Á. Một vật liệu có tính axit đã được lấy đến từ benzoin bằng cách thăng hoa và được đặt tên là “hoa của benzoin”, hay là axit benzoic. Do đó hydrocarbon có nguồn gốc từ axit benzoic thu đã được tên là benzin, benzol hoặc benzen. Michael Faraday lần đầu tiên phân lập , và xác định benzen vào năm 1825 từ dư lượng dầu có nguồn gốc đến từ việc sản xuất khí phát sáng, đặt cho nó cái tên bicarburet của hydro. Năm 1833, Eilhard Mitscherlich đã sản xuất nó chỉ bằng cách chưng cất axit benzoic (từ nhựa benzoin) và vôi. Ông đã đặt cho hợp chất tên chính là benzin. Năm 1836, nhà hóa học người Pháp Auguste Laurent đặt tên cho chất này chính là “phène”; đến từ này đã trở thành đến từ gốc của từ tiếng Anh “phenol”, đó là benzen đã được hydroxyl hóa và ” phenyl”, gốc tự do đã được hình thành do sự trừu tượng của một nguyên tử hydro (gốc tự do H •) từ benzen.
liên kết hỏng
Benzen – Wikipedia tiếng Việt
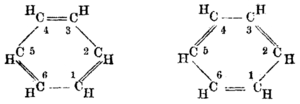
] chỉnh năm 1872 của Kekulé về lý thuyết năm 1865 của ông, minh họa sự thay đổi nhanh chóng của liên kết đôi [note 1]Điềuchỉnh năm 1872 của Kekulé về triết lý năm 1865 của ông, minh họa sự biến hóa nhanh gọn của link đôiNăm 1845, Charles Mansfield, thao tác dưới quyền August von von Hofmann, đã tách benzen từ nhựa than đá. Bốn năm sau, Mansfield mở màn sản xuất benzen ở quy mô công nghiệp tiên phong, dựa trên biện pháp than đá. Dần dần, ý thức tăng trưởng giữa những nhà hóa học rằng 1 số ít chất có tương quan về mặt hóa học với benzen, gồm có một họ hóa học phong phú. Năm 1855, Hofmann đã sử dụng đến từ ” thơm ” để chỉ định mối quan hệ mái ấm gia đình này, vì đặc thù đặc trưng của nhiều thành viên trong họ chất này. [ 11 ] Năm 1997, benzen đã được phát hiện trong khoảng trống liên sao. [ 12 ]
Công thức vòng
Công thức thực nghiệm cho benzen đã được biết đến từ lâu, nhưng cấu trúc không bão hòa cao của nó, chỉ với một nguyên tử hydro cho mỗi nguyên tử carbon, là thử thách để xác lập. Archibald Scott Couper năm 1858 và Joseph Loschmidt năm 1861 [ 19 ] đã yêu cầu những cấu trúc hoàn toàn có thể chứa nhiều link đôi hoặc nhiều vòng, nhưng sau đó có quá ít vật triệu chứng để giúp cho những nhà hóa học quyết định hành động bất kể cấu trúc đơn cử nào .Năm 1865, nhà hóa học người Đức Friedrich August Kekulé xuất bản một bài báo bằng tiếng Pháp ( khi đó ông đang giảng dạy tại vùng Bỉ sử dụng Pháp ngữ ) cho thấy cấu trúc benzen chứa một vòng gồm sáu nguyên tử carbon với những link đơn , đôi xen kẽ. Năm sau, ông xuất bản một bài báo dài hơn bằng tiếng Đức về cùng một chủ đề. [ 20 ] [ 21 ] Kekulé đã sử dụng chỉ bằng triệu chứng tích lũy trong những năm qua, đơn cử là, có vẻ như luôn luôn chỉ có một đồng phân của bất kể đơn chất hóa học nào của benzen , và luôn luôn Open đúng chuẩn ba đồng phân của mọi dẫn xuất bị vô hiệu., quy mô meta và para của sự thay thế sửa chữa arene để tương hỗ cho cấu trúc đề xuất kiến nghị của ông. [ 22 ] Vòng đối xứng của Kekulé hoàn toàn có thể lý giải những vấn đề gây tò mò này, cũng như tỷ suất carbon-hydro 1 : 1 của benzen .
Sự hiểu biết mới này về benzen, , và do đó của tất cả các hợp chất thơm, được chứng minh là rất nhiều quan trọng đối với cả hóa học tinh khiết , hóa học ứng dụng mà vào năm 1890, Hiệp hội Hóa học Đức đã tổ chức một sự đánh giá cao về khám phá của Kekulé, kỷ niệm năm thứ 25 của bài báo về benzen đầu tiên của ông. Ở đây Kekulé đã nói về việc gây nên lý thuyết. Ông nói rằng ông đã chỉ ra hình dạng chiếc nhẫn của phân tử benzen sau khi có tiếng vang hay giấc mơ ban ngày của một con rắn tự giữ đuôi của mình (đây chính là một biểu tượng phổ biến trong nhiều nền văn hóa cổ đại được gọi chính là Ouroboros hoặc nút thắt vô tận).[23] Tầm nhìn này đã đến với ông sau nhiều năm nghiên cứu bản chất của các liên kết carbon-carbon. Mất 7 năm sau khi ông giải quyết vấn đề làm thế nào các nguyên tử carbon có thể liên kết với tối đa bốn nguyên tử khác cùng một lúc. Thật kỳ lạ, một mô tả tương tự, hài hước về benzen đã xuất hiện vào năm 1886 trong một cuốn sách nhỏ có tựa đề Berichte der Durstigen Chemischen Gesellschaft (Tạp chí của Hiệp hội hóa học khát nước), một bản nhái của Berichte der Deutschen Chemischen Gesellschaft. một vòng tròn, thay vì rắn như trong giai thoại của Kekulé.[24] Một số nhà sử học cho rằng nhại lại là một cây đèn thần của giai thoại rắn, có thể được biết đến qua truyền miệng ngay cả khi nó chưa xuất hiện ở trên báo in. Bài phát biểu năm 1890 của Kekulé [25] trong đó giai thoại này xuất hiện đã được dịch sang tiếng Anh.[26] Nếu giai thoại là ký ức của một sự kiện có thật, thì các tình huống đã được đề cập trong câu chuyện nhận thấy nó phải xảy ra vào đầu năm 1862.[27]
Bản chất tuần hoàn của benzen sau cuối được xác nhận bởi nhà tinh thể học Kathleen Lonsdale vào năm 1929. [ 28 ] [ 29 ] Nhà hóa học người Đức Wilhelm Korner đã yêu cầu những tiền tố ortho -, meta -, para – để Nhận biết những dẫn xuất benzen thay thế sửa chữa trị vào năm 1867 ; tuy nhiên, ông chưa sử dụng những tiền tố để Nhận biết vị trí tương đối của những nhóm thế trên vòng benzen. [ 30 ] Đó là nhà hóa học người Đức Karl Gräbe, vào năm 1869, lần tiên phong sử dụng tiền tố ortho -, meta -, para – để biểu lộ những vị trí tương đối đơn cử của những nhóm thế ở trên một vòng thơm thay thế sửa điều trị di ( viz, naphthalene ). [ 31 ] Năm 1870, nhà hóa học người Đức Viktor Meyer lần tiên phong vận dụng danh pháp của Gräbe cho benzen. [ 32 ]
Ứng dụng khởi đầu
Trong thế kỷ 19 và đầu thế kỷ 20, benzen được sử dụng thực hiện kem dưỡng da sau cạo râu vì mùi dễ chịu , và thoải mái của nó. Trước những năm 1920, benzen thường được sử dụng thực hiện dung môi công nghiệp, đặc biệt quan trọng chính là để tẩy sắt kẽm kim loại. Khi độc tính của nó trở nên rõ ràng, benzen được sửa chữa trị thay thế bởi những dung môi khác, đặc biệt quan trọng là toluene ( methylbenzene ), có đặc thù vật lý tựa như nhưng không gây ung thư .Năm 1903, Ludwig Roselius đã phổ cập việc sử dụng benzen để khử caffein cafe. Phát hiện này đã dẫn đến việc sản xuất Sanka. Quá trình này sau đó đã bị ngưng. Benzen trong lịch sử vẻ vang được sử dụng như một thành phần quan trọng trong nhiều mẫu sản phẩm tiêu dùng như Cờ lê lỏng, một số ít công cụ cạo sơn, xi-măng cao su đặc, tẩy trang tại chỗ , những mẫu sản phẩm khác. Việc sản xuất một số ít công thức chứa benzen này đã ngừng vào khoảng chừng năm 1950, mặc dầu Cờ lê lỏng vẫn liên tục chứa một lượng đáng kể benzen cho đến cuối những năm 1970. [ 33 ]
Xuất hiện ngoài tự nhiên
Một lượng nhỏ benzen đã được tìm thấy trong dầu mỏ , và than đá. Nó là mẫu sản phẩm phụ của quá trình đốt cháy không trọn vẹn của nhiều vật tư. Đối với mục tiêu thương mại, cho đến Thế chiến II, hầu hết benzen được lấy thực hiện mẫu sản phẩm phụ của sản xuất than cốc ( hay là ” dầu nhẹ lò than ” ) cho ngành công nghiệp thép. Tuy nhiên, trong những năm 1950, nhu yếu về benzen tăng lên, đặc biệt quan trọng là đến từ ngành công nghiệp polymer đang tăng trưởng, yên cầu phải sản xuất benzen từ dầu mỏ. Ngày nay, hầu hết benzen đến từ ngành công nghiệp hóa dầu, chỉ có một phần nhỏ được sản xuất từ than đá. [ 34 ]
Cấu trúc phân tử
 Cấu trúc phân tử benzenCấu trúc mà Kekulé đưa ra hầu hết chưa thuyết phục đã được những nhà khoa học đương thời, vì địa thế căn cứ vào công thức phân tử thì phân tử benzen biểu lộ tính không no cao nhưng rất khó tham gia phản ứng cộng, ngược lại benzen rất nhiều dễ tham gia phản ứng thế. Tuy vậy vào năm 1929, công thức của Kekulé được công nhận bởi Kathleen Lonsdale .
Cấu trúc phân tử benzenCấu trúc mà Kekulé đưa ra hầu hết chưa thuyết phục đã được những nhà khoa học đương thời, vì địa thế căn cứ vào công thức phân tử thì phân tử benzen biểu lộ tính không no cao nhưng rất khó tham gia phản ứng cộng, ngược lại benzen rất nhiều dễ tham gia phản ứng thế. Tuy vậy vào năm 1929, công thức của Kekulé được công nhận bởi Kathleen Lonsdale .
Theo phân tích quang phổ thì góc liên kết giữa các nguyên tử trong benzen đều là 120 độ, các liên kết C-C đều như nhau (140 pm), lớn hơn liên kết đôi đơn lẻ , nhỏ hơn liên kết đơn (136 pm , 147 pm). Điều này được giải thích qua thuyết lai hoá obitan như sau: trong phân tử benzen, các nguyên tử C ở trạng thái lai hoá sp2 liên kết với nhau , và với các nguyên tử H thành mặt phẳng phân tử benzen, các obitan p vuông góc với mặt phẳng không những liên kết thành cặp mà liên kết với nhau thành hệ liên hợp. Do vậy mà liên kết đôi ở benzen thường bền hơn so với các hợp chất có liên kết đôi khác, dẫn đến các tính chất đặc trưng mà người ta gọi chính là tính thơm.
Phản ứng cộng
Benzen trong điều kiện có xúc tác niken, nhiệt độ cao cộng với khí hydro tạo ra xiclohexan. Khi có chiếu sáng, benzen tác dụng với khí clo gây ra hexacloran C6H6Cl6 (còn gọi chính là thuốc trừ sâu ba số 6, thuốc trừ sâu 6-6-6), một thuốc trừ sâu hoạt tính rất nhiều mạnh, đã bị cấm. ===
Khi có Axit Lewis, benzen phản ứng với methylclorua tạo ra toluen .Ngoài ra, benzen hoàn toàn có thể được chuyển thành nhiều hợp chất khác theo cách này. Ví dụ như amphetamine :C6H6 + CH2 = CH-CH2Cl -> C6H5CH2CH ( CH3 ) Cl ( xúc tác AlCl3 )C6H5CH2CH ( CH3 ) Cl + NH3 -> C6H5CH2CH ( CH3 ) NH3 + Cl -Thuỷ phân các loại sản phẩm, thu đã được amphetamine .
Phản ứng thế electrophyl
Benzen phản ứng thế với halogen ( X2 ) khi có sắt hoặc axit Lewis ( AlCl3 ) tạo phenyl halide ( C6H5X ), phản ứng với axit nitric đặc có xúc tác axit sulfuric đậm đặc tạo nitro benzen ( trong điều kiện kèm theo ngặt nghèo hơn – axit bốc khói và nhiệt độ cao – sinh ra TNB ), phản ứng với axit sulfuric đậm đặc chưng cất nước thành axit benzosulfonic. Quy tắc chung được nêu trong hình dưới .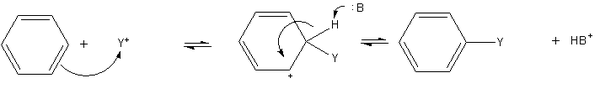 Phản ứng thế trong nhân thơmNếu như có thêm nhóm thế thì phản ứng thế vào nhân thơm cũng sẽ nhanh hơn hoặc chậm hơn tuỳ vào thực chất nhóm thế :
Phản ứng thế trong nhân thơmNếu như có thêm nhóm thế thì phản ứng thế vào nhân thơm cũng sẽ nhanh hơn hoặc chậm hơn tuỳ vào thực chất nhóm thế :
Dạng định hướng đồng phân Nhóm thế tiêu biểu Mức độ Hoạt hoá/Phản hoạt hoá
Định hướng ortho, para – OH, – NH2 (-NHR, -NR2) Mạnh Hoạt hoá
– OR Trung bình
– NHC(R)=O
– OC(R)=O
– R, – Aren
– X (halogen)
Yếu Phản hoạt hoá
Định hướng meta -C(R)=O, – CH=O
– COOH, – C(NH2)=O
– COOR
-SO3H, – CN, – CF3 Trung bình
-NO2, -NR3, -SR3 Mạnh
Trùng hợp Acetylen
3 CH = CH — C, 6000 — > C6H6
Dùng Axit Benzoic
Cho axit benzoic công dụng với natri hydroxide theo phản ứng :C6H5COOH + 2 NaOH — > C6H6 + Na2CO3 Benzen có mùi thơm dễ chịu , và thoải mái giống mùi bánh ngọt vừa nướng xong, nhưng mùi này có hại cho sức khoẻ ( gây bệnh bạch cầu ). Ngoài ra, khi hít Benzen vào, hoàn toàn có thể gây vô sinh, cần quan tâm khi tiếp xúc trực tiếp với Benzen. Có thể gây bệnh ung thư máu. Benzen khi rơi vào da sẽ gây bỏng rát
Đồng phân vị trí nhóm thế
Nếu có hai nhóm thế đính vào nhân thơm thì cho ra 3 đồng phân: thế 1,2- chính là ortho- (o-), thế 1,3- là meta- (m-), thế 1,4- chính là para- (p-).
Ngày nay một lượng lớn benzen chủ yếu để:
Sản xuất styren cho tổng hợp polymer.Sản xuất cumen cho việc sản xuất cùng lúc axeton , phenol.Sản xuất cyclohexan tổng hợp tơ nilon.Làm dung môi, sản xuất dược liệu.
Các dẫn xuất và đồng đẳng
Toluen: có được từ chưng cất nhựa than đá hoặc cho benzen phản ứng với metylclorua có axit Lewis, ứng dụng chính là sản xuất thuốc nổ TNT , thực hiện dung môi.Xilen: có ba đồng phân o-, m-, p-, chính là sản phẩm của quá trình chưng cất hoá dầu, dùng trong kỹ nghệ.Cumen: có đã được nhờ cộng benzen vào propen.dãy đồng đẳng của Benzen có công thức tổng quát CnH2n-6 với n ≥ 6 \ displaystyle n \ geq 6
Lỗi chú thích: Đã tìm thấy thẻ với tên nhóm “note”, nhưng không tìm thấy thẻ tương ứng tương ứng, hoặc thẻ đóng
bị thiếu

