Cung cấp sản phẩm, dịch vụ với chất lượng cao, không có hàng hư, hàng lỗi là ưu tiên hàng đầu của tất cả các doanh nghiệp. Chính vì vậy mà việc phát hiện giải quyết vấn đề trong tổ chức là một điều cực kì quan trọng. Và yêu cầu này là đặc biệt quan trọng đối với sản xuất dược phẩm, thiết bị y tế. Các nghành này đòi hỏi phải có một quy trình đảm bảo ằng các lỗi được điều tra và phân tích rõ gốc dễ, khắc phục hoàn toàn và ngăn ngừa lặp lại. Quy trình đó chính là CAPA– Corrective Action Preventive Action. Vậy CAPA là gì vậy? Vì sao đó là quy trình quan trọng cần phải thực hiện?

CAPA – Corrective Action Preventive Action là gì vậy?
CAPA là viết tắt của cụm từ Corrective Action Preventive Action, trong tiếng việt có thể dịch là “hành động khắc phục và phòng ngừa”. CAPA là một yêu cầu của FDA- cục quản lý dược phẩm Hoa Kỳ (Food and drug Administration), C P cũng là một yêu cầu bắt buộc của EMA – cơ quan dược phẩm Châu u (European Medicines Agency), theo đó muốn xuất khẩu thuốc vào thị trường Mỹ hay Châu u bắt buộc phải có giấy phép sản xuất thực hành tốt sản xuất thuốc GMP và một số giấy chứng nhận quan trọng khác trong đó có CAPA. CAPA là một trong Các yêu cầu bắt buộc doanh nghiệp sản xuất dược phẩm phải đưa vào hệ thống quản lý chat lượng của họ.
Bạn đang đọc: Giải mã CAPA và Các ưu việt của nó
Giải mã CAPA và Các ưu việt của nó
CAPA bao gồm hai khía cạnh là CA- hành động khắc phục và PA – hành động ngăn ngừa. Trong các tiêu chuẩn EU GMP, FDA hai hành động này được đề cập cạnh tranh nhau, CA rồi đến PA. Nhiều người nhầm tưởng hai hành động này là một chuỗi đi cùng nhau. Tuy nhiên, với trên thực tế thì chúng lại riêng biệt và PA thậm chí nên đi trước sau đó tới PA. Tức là phòng ngừa trước các lỗi, sự cố có thể xảy ra rồi mới đi khắc phục và đưa ra phòng ngừa cho sự lặp lại.

CA ( Corrective Action ) – hành động khắc phục là gì vậy?
CA là hành vi vô hiệu nguyên do nền tảng của sự không tương thích hoặc thực trạng không mong ước hiện có để ngăn ngừa sự tái phát. Có thể nói CA là sự lan rộng ra của kỹ thuật nghiên cứu và phân tích nguyên do căn nguyên ( RAC ). Bởi tiềm năng của CA là tìm ả được u nhọt của yếu tố. Rồi liên tục triển khai hành vi vô hiệu căn nguyên .

Ví dụ như khi lũ lụt, mực nước biên dâng cao bạn khắc phục bằng Các xây Các con đê chắn. Tuy nhiên đây chỉ là Các hành vi tức thời. Gốc dễ của nó là sự đổi khác khí hậu, chặt phá rừng .. giải quyết và xử lý hàng loạt Các nguyên do đó thì đó gọi là hành vi khác phục .
PA ( Preventive Action) – hành động phòng ngừa là gì vậy?
Xem thêm: Nghĩa Của Từ Cote Cao Độ Trong Xây Dựng là gì vậy ? Cao Độ Trong Xây Dựng là gì vậy
PA – Preventive Actionlà loại bỏ các nguyên nhân tiềm ẩn để ngăn chặn sự suất hiện của nó. Hành động ngăn ngừa phải được thực hiện trước khi lỗi xảy ra.
Lấy lại ví dụ bên trên, với kiểm tra mức độ ô nhiễm, thực trạng phá rừng, sự nóng lên toàn thế giới .. so sánh và cảnh báo nhắc nhở .. thì đó là hành vi phòng ngừa .

Tại sao phải thực hiện CAPA – Corrective Action Preventive Action
Nhận diện nguyên do nền tảng của một sự thất bại là nguyên tắc chính của một mạng lưới hệ thống quản trị chất lượng thuốc ( PQS ). Khi một yếu tố xảy ra, cái mà ta thấy khởi đầu thường chỉ là một triệu chứng của yếu tố thực sự. Các triệu chứng đó hoàn toàn có thể được điều trị. Tuy nhiên, với nó hoàn toàn có thể tái nhiễm thậm chí còn lây lan bất kể khi nào. Hiểu được tại sao lại có triệu trứng này, xử lý triệt để và ngăn ngừa tái nhiễm mới lac mục tiêu thực sự của việc triển khai CAPA . Thêm vào đó, như đã đề cập CAPA là một nhu yếu bắt buộc của FDA, EMA. Cho nên, với việc không thực thi đúng quá trình C P là một khoanh vùng phạm vi của FDA. Điều này cực kỳ có ý nghĩa so với nghành sản xuất thực phảm, dược phẩm và thiets bị y tế thị trường Mỹ và Châu u .
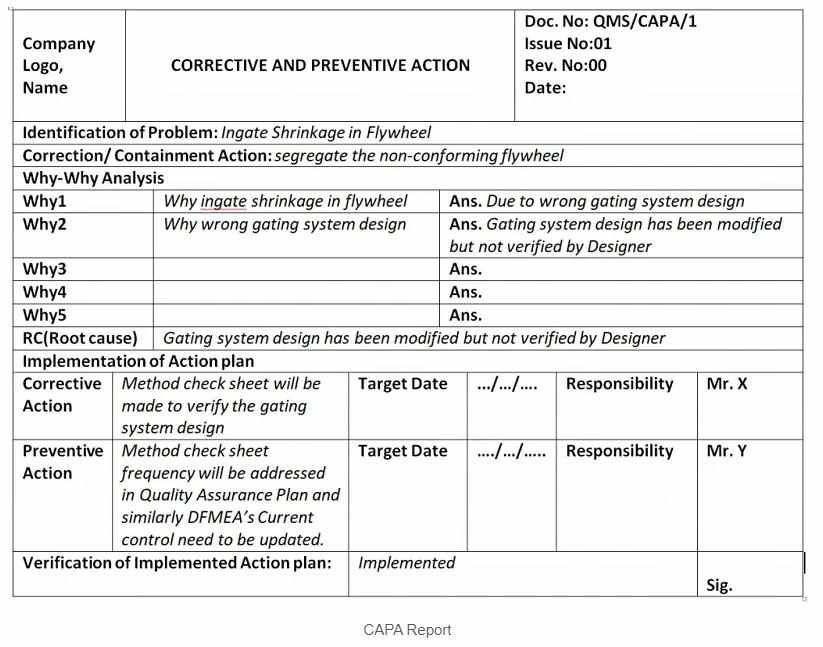
Báo cáo CAPA – Corrective Action Preventive Action